随着科学技术的不断进步,神经科学领域已涌现出多种技术方法,用于揭示大脑复杂功能的奥秘。这些方法包括在体多通道电生理、双光子钙成像、膜片钳、fMRI、PET等,每种技术都有其独特的优势和局限性。在这里我们将比较这些不同的神经生物学研究方法,探讨它们在神经科学研究中的应用和限制。通过对比分析,我们可以更好地理解如何选择合适的方法来研究特定的科学问题,以及如何综合不同方法的数据来获得更全面的洞见。
1 常用技术方法
多通道在体电生理记录通过多个微型化的电极阵列,能够在活体动物中同步记录不同脑区的生物电活动,捕捉精细的神经元动作电位和局部场电位。
单光子/双光子钙成像技术通过表达遗传编码的钙指示蛋白,将神经元活动时的钙离子浓度波动,表现为可以被信号检测设备记录到的强度变化。
膜片钳技术通过将玻璃微电极与细胞膜表面紧密接触,利用负压吸引形成高阻抗封接,电学上隔离一小片细胞膜。在此基础上,可以通过施加电压或电流,控制并监测细胞膜上离子通道的活动。
fMRI通过血氧水平依赖效应,即BOLD效应,来检测大脑活动。当神经元活跃时,消耗氧气并释放二氧化碳,引发局部血流量增加,从而改变血液的磁化特性。这种变化被高灵敏度的MRI设备检测到,经过数据处理,生成激活图。PET通过注射正电子发射放射性标记的分子探针,这些分子探针会聚集在特定组织或器官中。当它们衰变时,会产生正电子,与电子相撞后释放能量,被探测器捕捉,经过计算机处理生成清晰图像。
2 记录特征比较
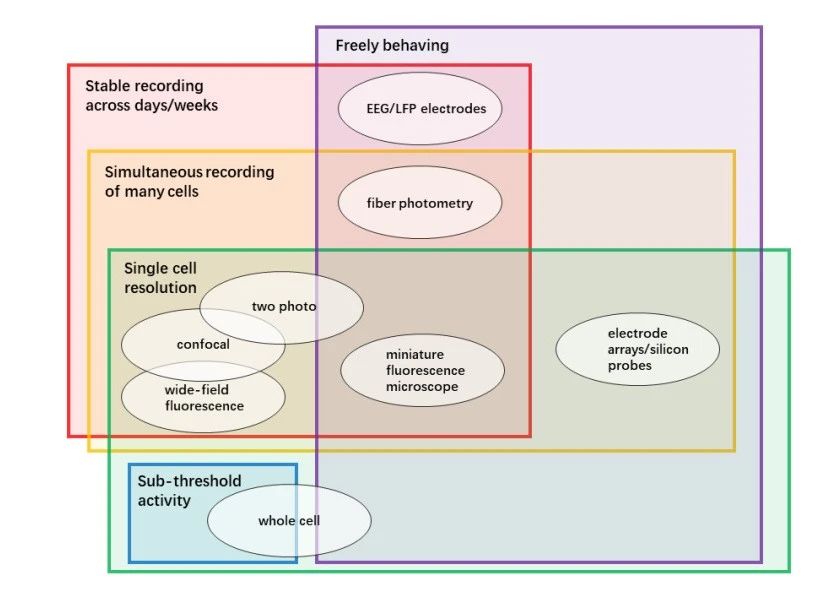
在记录特征方面,膜片钳技术具有极高的敏感性,能够捕捉到单个神经元动作电位阈值之下的微小膜电位波动。然而,这种记录方法仅限于脑片实验,无法全面反映活体突触连接的复杂性。此外,膜片钳技术一次只能记录一个或少数几个神经元的活动。相比之下,EEG/LFP和光纤记录技术可以在自由活动的动物上获取脑区群体神经元的整体活动特征。这些方法可以持续数天甚至数周,但它们无法区分单个神经元的活动特点。近年来,多通道在体电生理技术和小型化的单光子内窥镜技术(如miniscope)取得了显著进展。这些技术综合了上述优点,能够在活体动物上长时间记录数十甚至数百个神经元的活动。此外,近几年还开发出了小型化的双光子和三光子在体显微镜,这些显微镜不仅重量极轻,可让小鼠在自然行为条件下佩戴,而且能够获得更清晰、更大群体的神经元钙活动图像。这些先进的成像技术为神经科学研究提供了前所未有的视和具,使得可视化研究大脑深部结构的神经机制成为可能。
3 时空分辨率比较
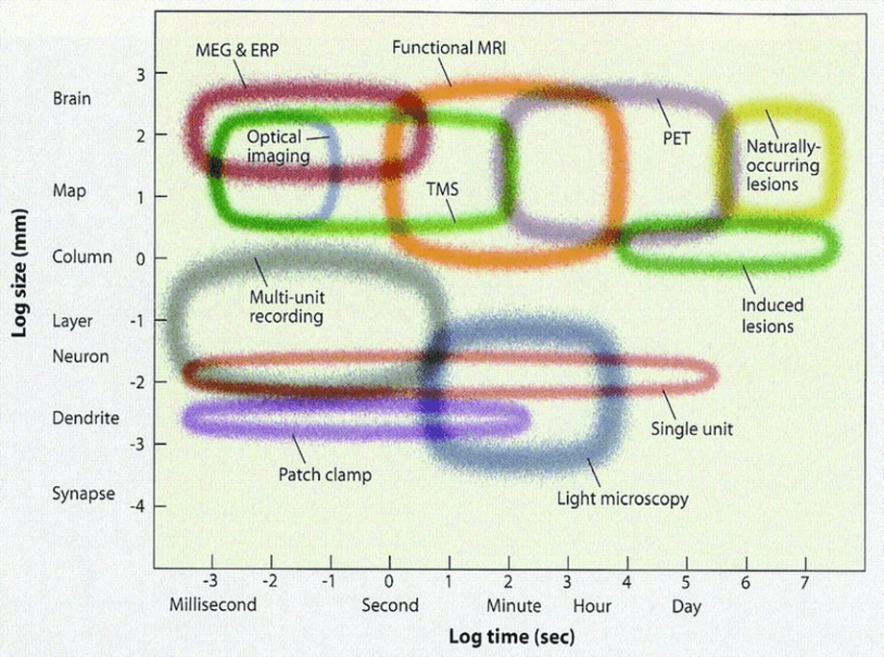
在选择适合的研究工具时,我们通常需要根据研究所需的时空分辨率来决定。fMRI(磁共振成像)通过利用磁场和射频脉冲来生成人体内部的详细图像,它能够揭示大脑的结构、功能以及代谢等生理过程,并用于诊断和评估某些神经系统疾病。PET(正电子发射断层扫描)则通过体内注射含有放射性同位素的药物,利用正电子与电子相互作用产生的伽马射线进行成像,它可以帮助我们研究大脑的代谢、血流和受体分布等生理过程,并用于诊断和评估某些神经系统疾病。然而,尽管MRI和PET等技术能够提供全脑的活动特点,但在时空分辨率上却显得严重不足。fMRI能够检测到大脑活动的变化,但由于血流动力学反应的延迟,无法实时反映神经元的活动,一般来说,fMRI的时间分辨率约为2-3秒,空间分辨率通常在1-3毫米之间;而由于PET成像依赖于放射性示踪剂的分布和代谢过程,导致其反应速度较慢,时间分辨率通常在几分钟的范围内,空间分辨率通常在4-8毫米之间。
在时空分辨率方面,多通道记录、钙成像和膜片钳等技术则具有显著优势。在体多通道记录能够在神经元水平上轻松达到毫秒级的时间分辨率,我们常用的记录频率为30kHz或40kHz。双光子钙成像选用合适的钙成像荧光分子(如GCaMP7b),可以记录到突触水平的钙离子波动。膜片钳记录技术是一种高度灵敏的电生理学方法,它可以在亚毫秒级别的时间内检测到单个离子通道的开放和关闭。这种技术的优势在于其极高的时空分辨率,能够精确地测量离子通道的活动,从而帮助我们深入了解神经元的电生理特性和信号传导机制。与其他电生理学方法相比,膜片钳记录技术具有更高的灵敏度和准确性。
4 在体多通道记录
在体多通道电生理记录技术的原理主要基于神经元电活动的检测和信号转换。被植入到特定脑区的微型电极阵列非常灵敏,能够捕捉到神经元附近的电信号变化,当神经元被激活时,其膜电位的变化会导致电流的微小变动,这些微小的电信号被电极尖端捕捉,通过外部的数据采集系统放大后转换成数字信号,储存到本地便于后续分析。
使用四电极技术能够在多个电极触点上同步采集神经元的放电波形。每个神经元的放电活动会被四根电极同时采集。由于不同空间位置上的神经元与四根电极的距离不同,导致各电极上记录到的同一神经元的动作电位波形幅度不同。利用数学分类方法,如主成分分析(PCA)、独立成分分析(ICA)或聚类算法,根据波形特征和幅度差异对信号进行分类。通过上述分类,便可以区分记录电极周围每个神经元的放电。四电极技术提高了对单个神经元的空间分辨率,确保精确获得单个神经元的放电信息。
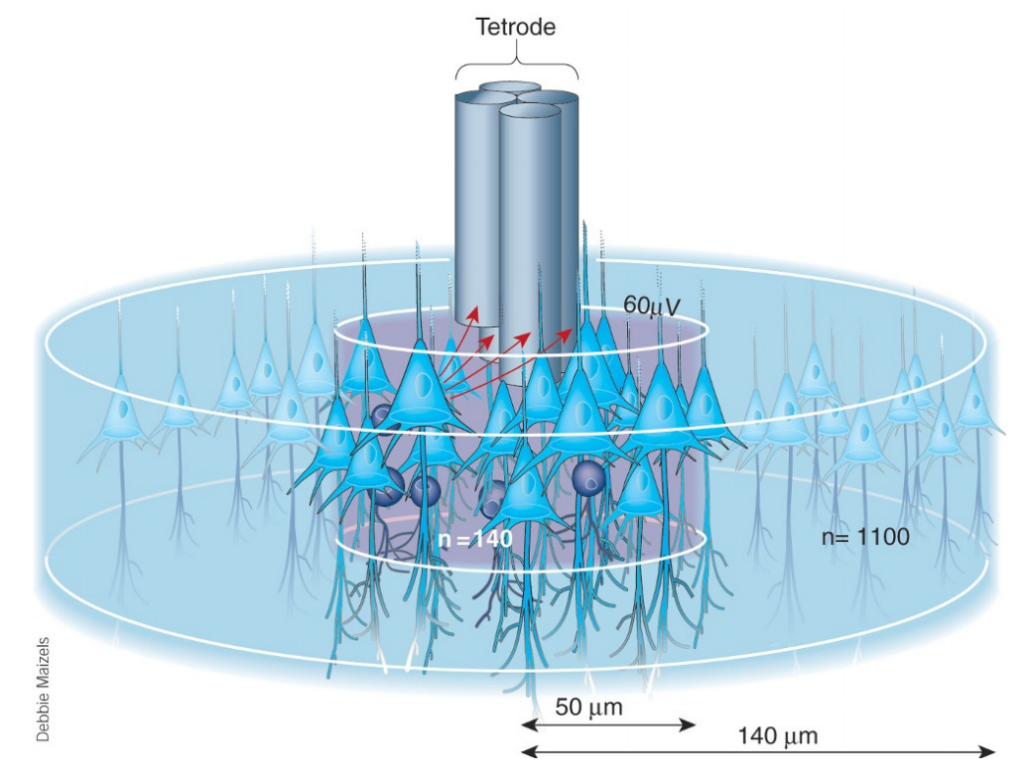
在体多通道电生理记录的核心优势在于其能够同步监测数十个神经元的活动。与传统的单通道记录相比,多通道记录技术可以同时捕捉到多个神经元的放电模式,这为研究神经网络中复杂的相互作用提供了可能。此外,这种技术能够捕捉到的电信号类型不仅限于单个神经元的动作电位,还包括局部场电位,这是一组神经元的集体响应,能够反映出大脑某区域的活动状态。
5 单光子钙成像
在体单光子钙成像技术,主要是基于荧光显微成像的技术。通过特异性的钙离子指示剂,例如GCaMP系列来标记神经元,钙离子指示剂能够与钙离子结合并产生荧光信号。一旦该神经元被激活,细胞内的钙离子浓度便会上升,这会使得指示剂的荧光强度增加。这种荧光变化可以被高灵敏度的光电探测器捕捉到,从而实现实时观察和记录神经元的活动。根据需要记录的不同脑区不同种类神经元的放电特征,可以选择不同的GCaMP类型。以GCaMP7系列为例,GCaMP7f(“fast”)适用于检测高频放电的神经元;GCaMP7s(“sensitive”)具有更敏感的动力学表现;GCaMP7b(“bright”)可以用于神经树突的成像;而GCaMP7c(“contrast”)则因其较低的静息荧光强度,适合大范围的成像。
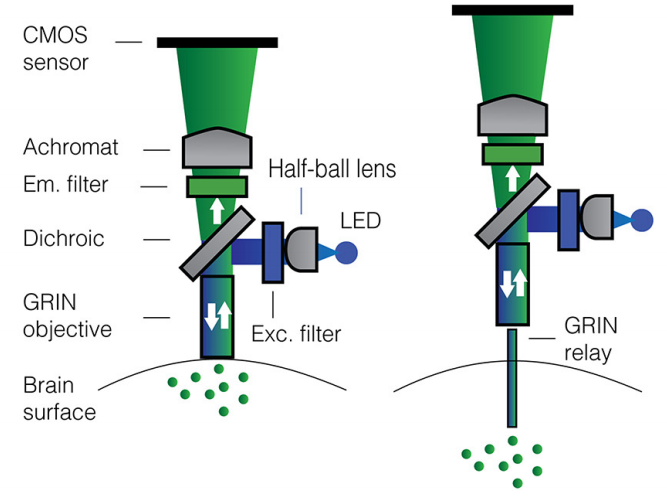
采集到的荧光信号随后需要进行复杂的数据处理和分析,这包括背景噪声的滤除、单个神经元信号的提取以及与行为数据的同步对比等。在处理这些数据时,可以选择使用一些现成的程序包来辅助工作。例如,NoRMCorre可用于消除运动噪声,CNMF_E能够提取单个神经元的活动,而CellReg则可以实现在多个记录文件中追踪观察同一细胞。
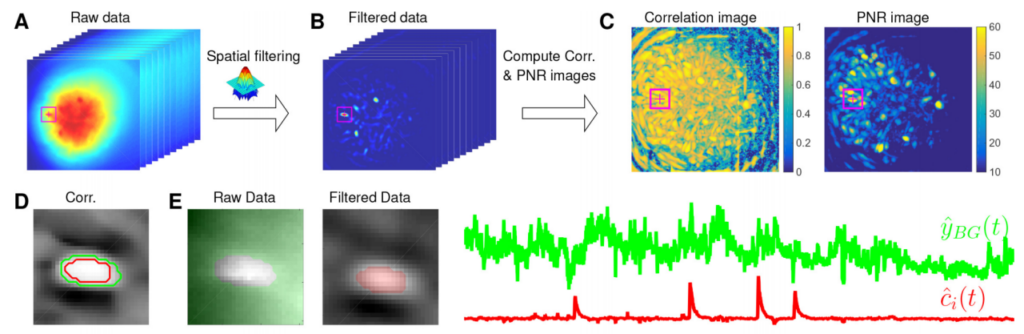
在体单光子钙成像技术具备高空间分辨率的显著优势,能够精准地同时追踪数百个神经元的活动,并支持在不同脑区进行多通道记录。此外,它特别适合于长期反复的观测,有助于深入研究神经环路在复杂行为中的功能动态。尽管在体单光子钙成像技术具有这些优点,但它也存在一些局限性。首先,这种技术的时间分辨率相对较低,通常仅能达到数十赫兹的采样率。其次,这项技术要求基因编码的指示剂必须在特定的神经元中表达,而这一过程可能会改变细胞的正常生理状态或引发免疫反应。再者,荧光信号的强度会受到多种因素的影响,包括指示剂的表达水平、细胞内环境的变化等,这些都可能对结果的准确性造成影响。此外,对于深度脑组织的成像,由于光信号穿透力的限制,通常需要采用侵入性的GRIN lens才能实现深脑区的成像,这可能会对脑组织造成一定的创伤。综上所述,在体单光子钙成像技术虽然具备显著的优势,但在应用过程中也需要注意其局限性,并结合其他技术手段来弥补其不足。
6
参考文献
[1]Aharoni, D. and T. M. Hoogland (2019). “Circuit Investigations With Open-Source Miniaturized Microscopes: Past, Present and Future.” Front Cell Neurosci 13: 141.
[2]Buzsaki, G. (2004). “Large-scale recording of neuronal ensembles.” Nat Neurosci 7(5): 446-451.
[3]Chen, T. W., et al. (2013). “Ultrasensitive fluorescent proteins for imaging neuronal activity.” Nature 499(7458): 295-300.
[4]Dana, H., et al. (2019). “High-performance calcium sensors for imaging activity in neuronal populations and microcompartments.” Nat Methods 16(7): 649-657.
[5]Wallace, D. J. and J. N. D. Kerr (2019). “All the light that we can see: a new era in miniaturized microscopy.” Nat Methods 16(1): 9-11.
[6]Zhao, C., et al. (2023). “Miniature three-photon microscopy maximized for scattered fluorescence collection.” Nat Methods 20(4): 617-622.
[7]Zhou, P., et al. (2018). “Efficient and accurate extraction of in vivo calcium signals from microendoscopic video data.” Elife 7.
[8]Jog, M.S. et al. (2002).”Tetrode technology: advances in implantable hardware, neuroimaging, and data analysis techniques.” J. Neurosci. Methods 117, 141–152 .
本文作者:侯佳佳|华东师范大学
邮箱:52271300017@stu.ecnu.edu.cn
欢迎沟通交流!

发表回复