引言
神经系统的功能有四:收集信息,编码信息,传递信息和存储信息,四者都选取电信号作为信息的主要载体。理论上来说,将任意导体插入大脑中,我们都能读取到相应区域的神经细胞电活动,而在采集到高质量的电信号后,科学家们需要对其做出解读,为此,我们必须先厘清这些电信号的来源和传递规律。
01
电信号的本质:离子移动
在任意时刻,脑中都充盈着大量的带电离子,离子的快速移动形成电场,这种移动常发生在膜结构内外(膜结构包括神经元的树突棘、树突、胞体、轴突和轴突末端等)。
值得一提的是,在谈论神经电活动时,人们常忽略神经胶质细胞的作用,神经元和胶质细胞间的互动是胞外低频电位的重要组成部分[1]。为了减少歧义,我们先对齐几个基本概念。
1)电场:向量,电场中一电场强度的值的单位是牛顿/库仑或伏特/米,电场的方向指向电势降低最快的方向(正电荷在电场中的受力方向);
2)电位:电场中的一个标量,常用V(标量)来表示;
3)电导率:张量,用于描述材料允许电荷载流子(如电子或离子)通过的难易程度;
4)局部场电位(Local Field Potential, LFP):在神经组织中,特定脑区一小群神经元活动所产生的电位变化。LFP是经由胞外记录技术测量得到的,能够反映神经元群体的综合电活动;5)Spike:神经元快速、短暂的电位变化。Spike可以通过电极直接测量,能反映单个或少量神经元的活动状态。
02
胞外电场最重要的影响因素:突触部位电活动
突触是神经元间传递信息的结构基础,其附近区域的离子移动既高频又高效。一个神经元上有数百到数万个突触(小脑中的浦肯野细胞有着繁茂的树突,单个浦肯野细胞大约能形成十万个突触)。由此,突触部位的电活动成为了胞外电场最重要的影响因素[2]。
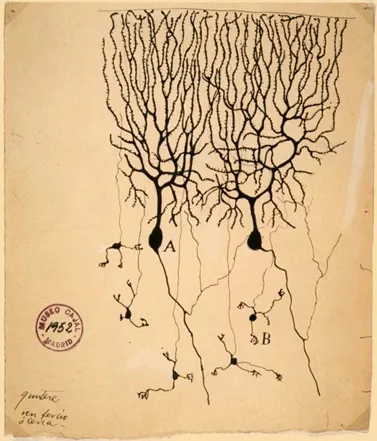
为了更好地描述神经元周围电场的活动,科学家们将正离子大量流入神经元的位置命名为“汇(sink)”,将正离子大量流出神经元的位置称作“源(source)”。
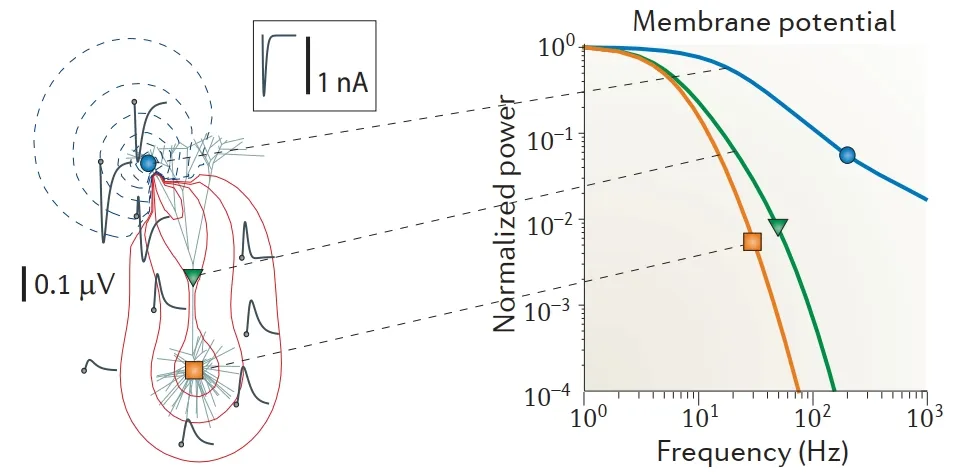
图 2 顶树突接受兴奋性传入后的神经元胞外电场变化(图2-图6均来自综述文章《The origin of extracellular fields and currents—EEG, ECoG, LFP and spikes. Nature reviews neuroscience》)
上图左为一个皮层第五层锥体细胞,其顶树突接受到了一次兴奋性的电流输入,由此诱发了顶树突胞外大量正离子内流——创造出了sink(蓝色虚线圆环);神经元需要一直维持电中性,因此,我们紧跟着就能在中段树突和胞体附近发现大量正电荷正在流出神经元,这些正电荷流出的区域即为source(红色实线环)。在电学中,sink和source常被称作“汇极”和“源极”,而邻近的源极和汇极能构成一个“双极子”(dipole),二者之间会产生较大的电流,进一步诱发电位变化。另外,图1右表明,记录区域距离突触部位(蓝色小圆)越远,胞外电位中的高频段就越少,大量生理过程和生理功能正是由高频段胞外电位来介导的。
扩展阅读——神经元电中性(Electroneutrality):在任一时间点,神经元局部区域可能会出现正负电荷富集的情况,但整个神经元始终呈电中性,即在每一个时刻,进入和流出神经元的电荷总量始终相等。在双极子中,汇极的负电区域会被源极区域迁移过来的正电荷快速“填充”,因此,双极子会极大地限制电流的传播距离(双极子内各区域电位与该区域到双极子中心距离的平方成反比);若源极和汇极相隔较远,则他们会分别形成一个单极子(monopole),单极子附近区域的电位值与该区域到源极或汇极中心的距离成反比。
03
胞外电位的组分:神经元动作电位
一个神经元上可以有多个突触同时被激活,诱发上文中提到的胞外电位变化,然而,一个神经元上却只有一个轴突始段,轴突始段处膜电位的快速逆转常会诱发剧烈的胞外电位变化,神经科学家们常将这种电位变化称作动作电位(Action Potential,AP)。
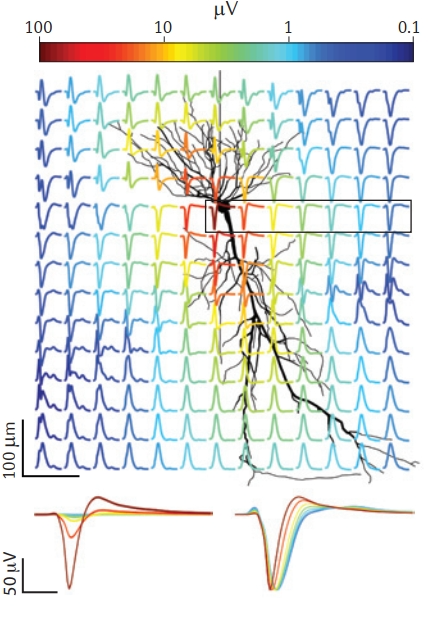
动作电位的持续时间为0.3-2ms,幅值变化为50-500μV[4]。下图展示了一个神经元轴突始段处爆发动作电位瞬间,胞外各区域的电位变化。在接受到树突传来的电位变化后,神经元轴突始段处大量阳离子(以钠离子为主)内流,胞外电位迅速变负,在同一层中(图3黑色方框划定的区域),胞外电位的变化幅度(图3下左)和速度(图3下右)随着记录位点到轴突始段距离的增加而迅速降低。
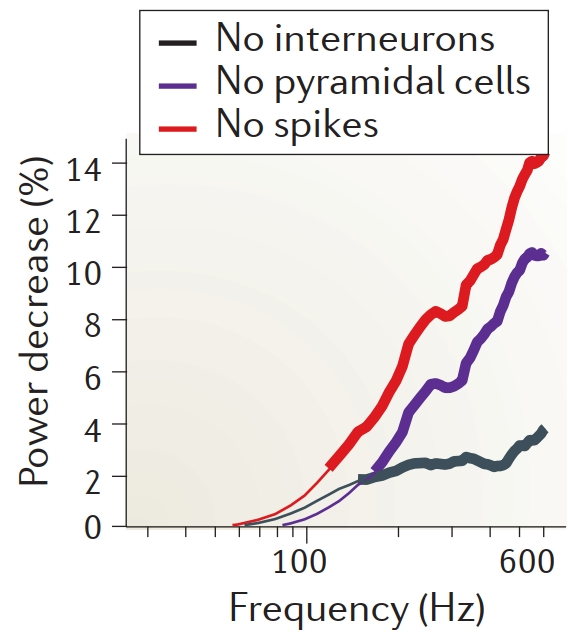
不仅如此,短时间内大量AP同步爆发也是胞外电位中高频段的重要来源。在将锥体细胞和中间神经元的spike信号去除后,胞外电位高频段的能量(波幅的平方)迅速衰减(图4)。
04
胞外电位的组分:钙离子spike
前文中我们只触及了突触部位电活动的皮毛,事实上,其中还有许多细节值得讨论,比如突触后膜上由钙离子内流诱发的spike,这种电活动也是胞外电信号的重要组分。
依据神经生物学的经典理论,突触后膜上的AMPA受体接受到前膜释放的谷氨酸后打开通道,钠离子进入胞内,有时也伴随NMDA受体激活后的钙离子内流,我们将这种阳离子内流引起的突触后膜电位变化称作一次兴奋性突触后电位(EPSP)。通常,单个EPSP持续时间只有几毫秒,电位变化幅度也很难超过5mV。然而,如果在较短时间内突触后膜同时产生多个EPSP,NMDA受体就会被激活,紧随其后,钙离子大量涌入胞内,胞内电位迅速上升10-50mV,这个过程可以持续10-100ms,神经科学家们常将这种电位变化称作“钙spike”[5]。图5为在胞外(上)和胞内(下)同时记录到的电位变化。虽然借助现有研究工具,我们很难从胞外电位中区分出单独的钙spike,但这并不妨碍其成为胞外电位不可或缺的影响因素。
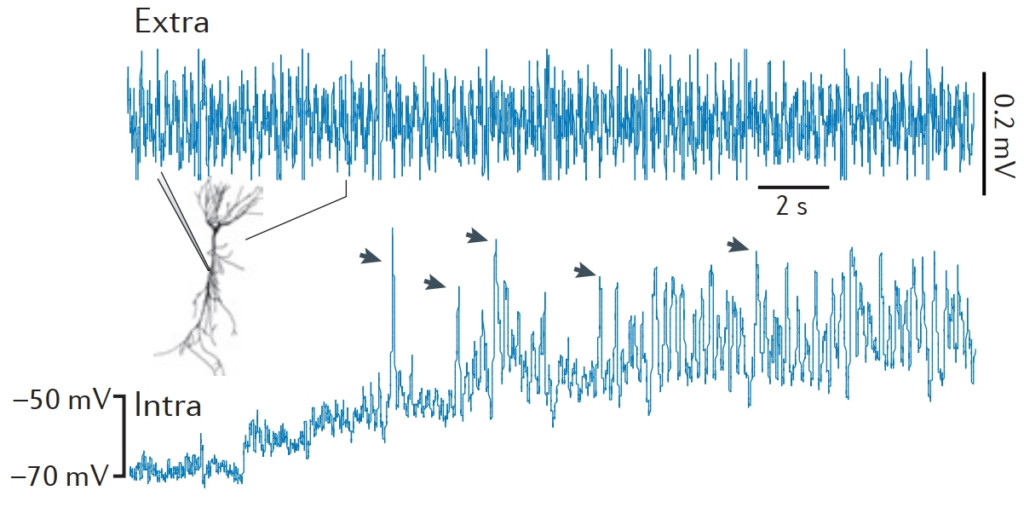
有意思的是,轴突始段由钠离子内流介导的AP常会发生倒流(back-propagating somatic action potentials),即动作电位经过胞体回流至树突,继而在树突上诱发钙spike[6]。
05
胞外电位的影响因素:神经元同步活动胞外电信号的记录方法决定了我们采集到的电位活动必然来自多个神经元的“合唱”,因此,在讨论完单个神经元胞外电位变化的诱发因素后,我们需要去关注神经元间的互动。
先来看一种被称作电场耦合(Ephaptic coupling)的现象,这是一种神经元间的非突触性相互作用,它不依赖于传统的化学突触[7]。在电场耦合中,一个神经元的电活动通过局部电场影响另一个神经元的膜电位。癫痫就是神经元高度同步放电的结果,而电场耦合被认为是癫痫产生的重要原因之一。胞外电位中的特征性节律同样来自神经元群体的同步活动。神经元在多个AP密集出现及其诱发的钙spike后常会进入到超极化状态(胞内电位比静息态更低),多个神经元同时出现这种状态时就会诱发周围电场的“down”状态。
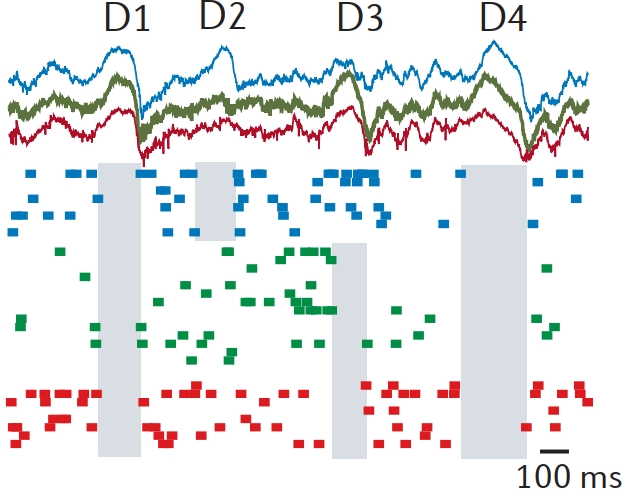
上图为在大鼠皮层区域采集到的睡眠时期的胞外电信号。锥体神经元群体同步去极化带来胞外电位的“up状态” ,而紧随其后的群体同步超极化则引发“down状态”,二者交替出现,构成了标志性的睡眠节律[8]。
扩展阅读:神经元自身的节律也会影响胞外电场。皮层区域的神经元常产生theta频段(4-12Hz)的自发放电,而对于胞体周围的中间神经元来说,它们常呈现统一的gamma频段(30-90Hz)共振。
06
胞外电位的影响因素:神经元的形态和排布
神经元的形态和排布同样会深刻地影响胞外电位。
长条形的神经元更容易形成偶极子,在偶极子中,电流的流动更为“充分”,由此带来的胞外电位波动也会更加剧烈;而外形近似圆形的神经元则更容易形成闭合电场closed field),闭合场中的电势差会被快速抹平,使其附近较难形成大电流。
扩展阅读:神经元树突具有低频滤波特性,起始于顶树突的一个100Hz的输入,在到达胞体后,其能量会衰减100倍,这为胞外电场的频率和能量成反比的现象提供了合理的解释[9]。
在啮齿类动物的皮层区域,多个神经元呈轴向平行分布,相当于并排放置了多个偶极子,这会带来叠加效应,并由此增大皮层处的胞外电位幅值;当神经元胞体分布在不同层,一个神经元的“源”往往会被周边神经元的“汇”迅速“吸收”,使得电流在小范围内快速抵消。由欧姆定律,在这些区域记录到的胞外电位也较小。
再来观察皮层的沟壑结构。相比沟壑的凸面,其凹面进一步拉近了并排排列的神经元胞体的间距,这使得沟壑凹面侧的电流密度普遍高于凸面,进而带来凹面侧更大的电位幅值。拉大视野——体积越大的物种,神经元胞体的分布越松散,这正是不同物种间胞外电位幅值差异的原因之一(胞外电位幅值:大鼠>猫>灵长类动物)[10]。
07
胞外电位的影响因素:体积传导为了定量计算胞外电场中某一点的电位,神经科学家们将脑组织简化成了一个各向同性的介质。整个脑组织中都充盈着电场,其中任一点的电导率σ被简化为一个标量,电导率的具体数值由该点的性质决定。我们可以利用麦克斯韦方程(忽略磁场的影响)计算某一点的电位:Ve = I / (4πσr),其中I为电流源的电流幅值,r为电流源和测量位点的距离。上述等式只考虑了一个电流源的情况,如果有多个电流源,则该点的电位为所有电流源效应的线性叠加。
体积传导(Volume conduction)是我们能在头皮外记录到深部脑区放电活动的根本原因[11]。在切除了一半的大脑后,实验人员仍能在“空洞”的头皮外记录到电信号,这些电信号就来自未被切除的那一半大脑胞外电活动的体积传导。扩展阅读:半脑切除(Hemispherectomy)通常涉及移除大脑的整个半球,包括大脑皮层和皮层下结构。这种手术是一种极端的神经外科手术,通常用于治疗严重的癫痫病例,尤其是当癫痫发作局限于大脑的一个半球,并且无法通过药物控制时[12]。
总结
为了深入解析神经元的编码机制,我们需要对胞外电位的产生和传播机制有深刻的理解。突触部位的电活动和轴突始段始段爆发的动作电位(AP)是胞外电位的重要组成部分。同时,神经元的同步活动、细胞的形态与排布、体积电导等多种因素,均会对胞外电位产生显著影响。在接下来的文章中,我们将继续探讨胞外电信号分析的基本原理及应用实例。参考资料[1] Poskanzer, K. E., & Yuste, R. (2011). Astrocytic regulation of cortical UP states. Proceedings of the National Academy of Sciences, 108(45), 18453-18458.[2] Niedermeyer, E., & da Silva, F. L. (Eds.). (2005). Electroencephalography: basic principles, clinical applications, and related fields. Lippincott Williams & Wilkins.[3] https://en.wikipedia.org/wiki/Purkinje_cell[4] Koch, C. (2004). Biophysics of computation: information processing in single neurons. Oxford university press.[5] Schiller, J., Schiller, Y., Stuart, G., & Sakmann, B. (1997). Calcium action potentials restricted to distal apical dendrites of rat neocortical pyramidal neurons. The Journal of physiology, 505(3), 605-616.[6] Bestman, J., Santos da Silva, J., Cline, H., Stuart, G., Spruston, N., & Hausser, M. (2008). Dendrite development. Dendrites, 2, 69-94.[7] McCormick, D. A. & Contreras, D. On the cellular and network bases of epileptic seizures. Annu. Rev. Physiol. 63, 815–846 (2001).[8] Steriade, M., Nunez, A., & Amzica, F. (1993). A novel slow (< 1 Hz) oscillation of neocortical neurons in vivo: depolarizing and hyperpolarizing components. Journal of neuroscience, 13(8), 3252-3265.[9] Lindén, H., Pettersen, K. H., & Einevoll, G. T. (2010). Intrinsic dendritic filtering gives low-pass power spectra of local field potentials. Journal of computational neuroscience, 29, 423-444.[10] Kahana, M. J., Seelig, D., & Madsen, J. R. (2001). Theta returns. Current opinion in neurobiology, 11(6), 739-744.[11] Buzsáki, G., Traub, R. D. & Pedley, T. A. in Current Practice of Clinical Encephalography (eds Ebersole, J. S. & Pedley, T. A.) 1–11 (Lippincott-Williams and Wilkins, 2003)[12] https://my.clevelandclinic.org/health/procedures/17092-hemispherectomy

发表回复