生物电活动属于一种极其微弱的电信号,非常容易受到干扰,因此要想记录到这种信号,就需要一套特定的放大系统。得益于电子工程技术的进步,目前在体电生理系统越来越小巧便携,但功能越来越强大,如支持的通道数更多,采刺一体,无线化,高精度,高信噪比等。一般情况,选择能够满足研究的系统组合即可。以下原则可以参考:
- 仅在术中进行,还是必须进行长期植入以满足研究;侧重记录单个单元的活动和峰值,还是对网络活动和振荡更感兴趣;
- 用于了解评估新技术发展的表现,还是调查神经科学研究问题;
- 仅用于基础研究,还是继续进行转化研究直至人体临床试验;
- 具体研究目的是什么:获取科学知识还是获取医疗器械批数据。
01
记录系统原理
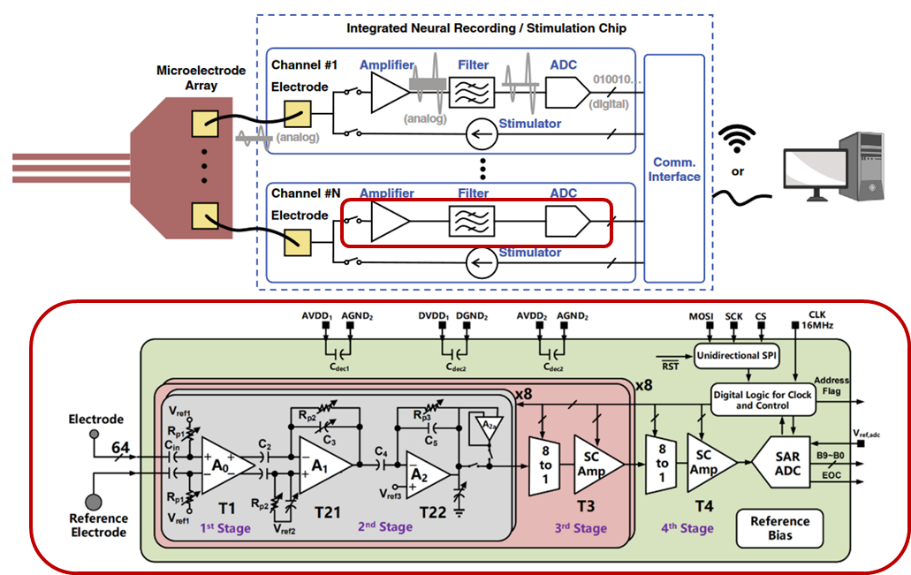
生物信号本身十分微弱,容易受到各种噪声干扰,在体记录就是需要把这种信号进行无失真的放大。概括而言,(1)输入:神经记录电极直接接触组织采集信号(记录电极见前文),(2)模拟前端预处理:信号放大、滤波、数模转换、数字信号处理;(3)显示:传输数据并最终显示、储存结果。
模拟前端(Analogue Front-End,AFE)是在体记录系统的核心,其设计决定了后续采集的信息类型以及精准度。这个与其所用放大器和数模转换核心的架构有关,常见的有低噪声放大器、斩波放大器;SARADC、增量式δ-σ ADC等。近年来,AFE中集成更多的功能,比如伪影抑制、spike检测、片上数据压缩等。同时,在微型化集成多个功能时,也受器件物理尺寸的限制,如电容密度,晶体管本身特性,高压(刺激功能)等2–4。
在设计AFE时需要满足一些要求:
- 最小功耗——为了确保使用安全,功耗必须始终低于80 mW/cm2。高功耗带来高温对组织也是一种严重的伤害5;
- 噪声性能——考虑到所采集信号的幅度较小,AFE必须具有出色的噪声性能。通过使用PMOS器件、JFET放大器或将输入信号上调至高于闪烁噪声的频率的斩波技术,可以部分或完全缓解这一问题6–8。
- 电极本身就是一个噪声源,AFE的噪声性能在设计时应考虑到电极的本底噪声,这样AFE本身的噪声性能就不会受到影响。过度设计,从而不必要地增加功耗。值得注意的是,电极的噪声性能取决于其几何和材料特性。因此AFE应设计为与特定电极配合使用,以获得最佳性能。
- 输入阻抗——AFE的输入级必须具有非常小的输入电容,因为EAP频段电极的传导机制本质上主要是电容性的,大的输入电容会导致信号衰减。
- 直流和低频抑制——由于记录电极会受到直流偏移和漂移的影响,因此有必要确保神经AFE包含高通滤波器来抑制这些。
- 最小尺寸——除了大规模扩展记录通道数量之外,还需要设计完全植入的记录设备,因此需要设计尽可能小尺寸的AFE。
更深入的就是不同模块中数字电路该如何设计、布局了,当然对于研究人员而言不需要了解太多。但需要了解系统的整体性能,比如噪声水平、功耗、带宽范围、精度等,这些对具体使用有一定的影响。一般认为高系统分辨率将允许与神经电路进行更精确和更全面的通信,从而更好地理解神经代码并解锁当前技术无法实现的许多潜在应用。例如一项研究表明,脑机接口可能需要同时记录多达5,000–10,000个神经元才能恢复肢体运动,并需要50,000–100,000个神经元才能长期实现“全身神经假体”9。分辨率广泛用于描述几个不同的方面,包括空间分辨率、时间分辨率和幅度分辨率,即可记录的神经元数量、采样精度,以及可精确量化的信号幅度。
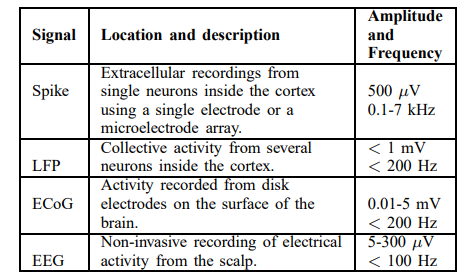
实际使用中根据研究的对象不同,需要选择不同的设备:如EEG幅度更小,关键频率更小,因此对系统的噪声设计水平、灵敏度要求更高;spike属于高频信号,幅值相对较大,因此对系统噪声水平容忍度较高,但频率相应范围和耐压范围需要更大。一般来说是无法混用的。
02
采集信号类型
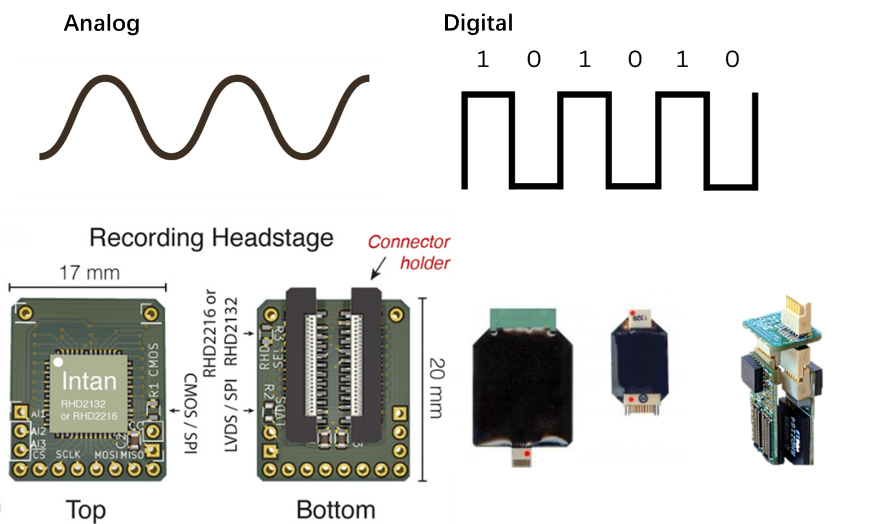
脑电本身是一种连续的非平稳信号,但我们最终采集到的数据是经数字化后的离散信号,这也是便于计算机处理,同时,数字信号抗干扰能力比模拟信号强。
集成了放大器和数模转换的小芯片我们称为Headstage。过去部分Headstage可以采用完全模拟放大器的形式,或者连接到模拟记录仪器或外部模数转换器(ADC),但如今的趋势是实现到数字域的转换作为Headstage的一部分。数模转换器和放大器分离的这种形式,信号从大脑出来后经过线缆传输到系统,这个过程中比较容易受到噪声干扰,影响信号质量;好处在于动物头部负担比较轻。目前多数是集成数模转换,可以直接连接在记录电极上,这样在传输阶段就是稳定的数字信号,并且可以降低传输线缆的数量。
模拟信号到数字信号只要采样率足够高,其中的关键信息就不会丢失,因此系统采样率是一个关键的参数。虽然奈奎斯特采样定理告诉我们,理论上二倍于最高频率进行采样,可以还原信号,但是还是建议使用10倍以上的采样率采集信号。另外一个就是数据的组织格式了,不同记录系统有百种记录格式,这一点其实并不友好。在数据分析一章中会细述。
03
记录形式
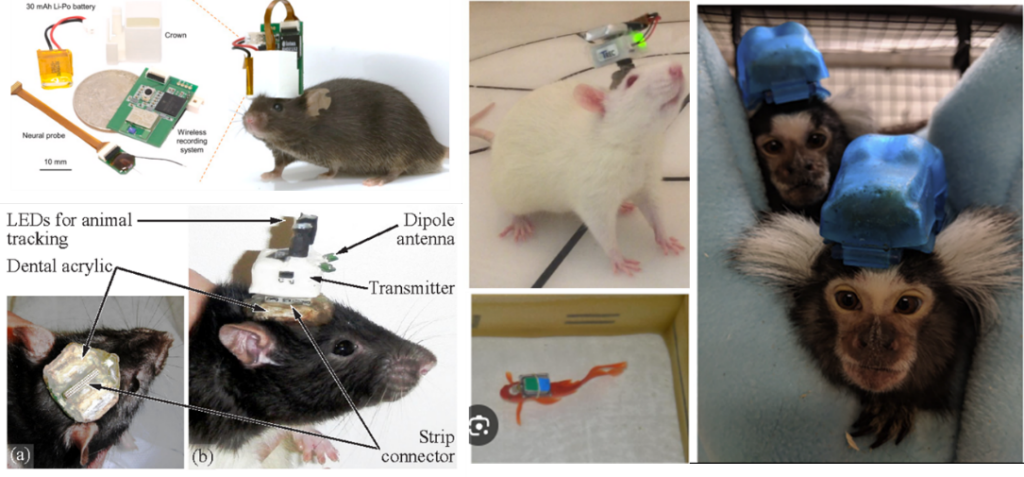
一般我们常用的记录系统都是有线记录系统,数据经预处理后的数据需要通过线缆传递到计算机进行后续处理。这种形式较为稳定,适合非常高通量的记录系统,如100 M/s以上的数据传输量。缺点即线材的束缚,在一定程度上会干扰被试者的状态。此外,还有无线记录系统。无线记录是一种很科幻的方式,目前无线记录仍然是比较小众,通道数不高,体积偏大。如果能更迷你一些,那就非常酷了。无线记录对功耗,高数据量的传输要求比较高,因此限制了发展。不过,未来技术突破有望改变这种情况,无线记录对情绪、社交、探索之类的研究还是很必要的。
04
记录系统要求
多数情况下采集阶段对电脑的要求不是很高,除非记录的通道非常高,如512通道以上。这种情况对硬盘,CPU,GPU都有一定要求,具体需要依据记录系统而定。不同的操作系统逻辑大同小异,首先需要设置一些参数,如采样率、降噪、阻抗测量、滤波参数、阈值、同步信号等,随后可以开始正常记录。同一实验务必保持一样的参数设置,方便后期数据分析。不少记录系统操作多从工程角度考虑,忽略了研究人员的使用习惯以及实际需求,因此也需要研究人员在一定程度上要进一步了解系统。
05
主要流程
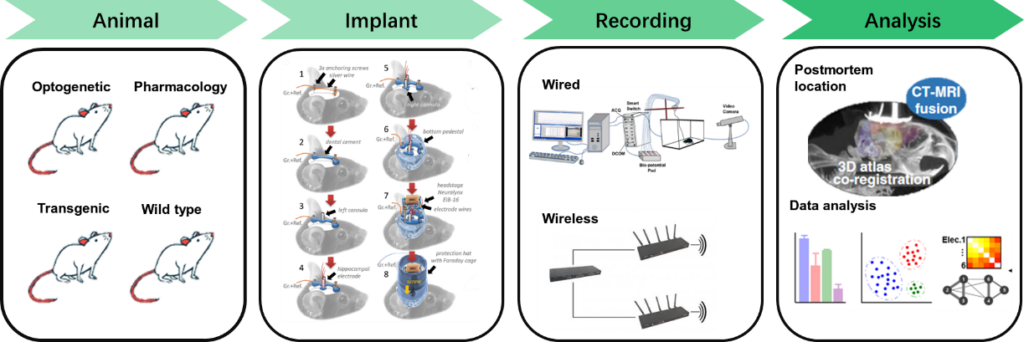
一般在体电生理的周期比较久,以慢性记录为例,需要提前准备好动物,规划脑区植入电极、恢复后进行记录并事后分析。其中记录阶段花费的时间最长,研究人员希望在保证科学的前提下尽可能多的采集数据。如果动物比较特殊,那么在准备阶段也需要较长的时间。
06
记录系统周边
记录大脑活动是为了解析内做或外在的变化,并通过干预进行因果验证,因此除了主要的记录系统外,在实际研究中往往还需要很多辅助的工具,比如激光器、电刺激器、行为箱、摄像头,有时需要研究人员自己动手设计和制作,这也是个有意思的地方。这个网站有不少工具可以参考(https://open-neuroscience.com/)。
最后分享一段spike的声音。
参考文献:
1.Zhang, X. et al. A Fully Integrated 64-Channel Recording System for Extracellular Raw Neural Signals. Electronics 10, 2726 (2021).
2.US20180193647A1 – System and method for charge-balancing neurostimulator with neural recording – Google Patents. https://patents.google.com/patent/US20180193647A1/en.
3.Yang, Z. et al. Neuronix enables continuous, simultaneous neural recording and electrical microstimulation. in 2016 38th Annual International Conference of the IEEE Engineering in Medicine and Biology Society (EMBC) 4451–4454 (2016). doi:10.1109/EMBC.2016.7591715.
4.US Patent Application for SYSTEM AND METHOD FOR SIMULTANEOUS STIMULATION AND RECORDING USING SYSTEM-ON-CHIP (SOC) ARCHITECTURE Patent Application (Application #20180199841 issued July 19, 2018) – Justia Patents Search. https://patents.justia.com/patent/20180199841.
5.Seese, T. M., Harasaki, H., Saidel, G. M. & Davies, C. R. Characterization of tissue morphology, angiogenesis, and temperature in the adaptive response of muscle tissue to chronic heating. Lab. Invest. 78, 1553–1562 (1998).
6.Ji, J. & Wise, K. D. An implantable CMOS circuit interface for multiplexed microelectrode recording arrays. IEEE J. Solid-State Circuits 27, 433–443 (1992).
7.ECoG Electrode Array with Embedded Coupling Capacitors for Area Efficient Neural Recording | IEEE Conference Publication | IEEE Xplore. https://ieeexplore.ieee.org/document/8584815.
8.A 2 μW 100 nV/rtHz Chopper-Stabilized Instrumentation Amplifier for Chronic Measurement of Neural Field Potentials. https://www.mrcbndu.ox.ac.uk/publications/2-mw-100-nvrthz-chopper-stabilized-instrumentation-amplifier-chronic-measurement.
9.Lebedev, M. A. & Nicolelis, M. A. L. Toward a whole-body neuroprosthetic. in Progress in Brain Research vol. 194 47–60 (Elsevier, 2011).
10.Mollazadeh, M., Murari, K., Cauwenberghs, G. & Thakor, N. From spikes to EEG: Integrated multichannel and selective acquisition of neuropotentials. in 2008 30th Annual International Conference of the IEEE Engineering in Medicine and Biology Society 2741–2744 (IEEE, Vancouver, BC, 2008). doi:10.1109/IEMBS.2008.4649769.
11.Mourão, F. A. G. et al. A Fully Adapted Headstage With Custom Electrode Arrays Designed for Electrophysiological Experiments. Front. Neurosci. 15, (2022).
12.A Wireless, Bidirectional Interface for In Vivo Recording and Stimulation of Neural Activity in Freely Behaving Rats (Video) | JoVE. https://app.jove.com/t/56299/a-wireless-bidirectional-interface-for-in-vivo-recording-and-stimulation-of-neural-activity-in-freely-behaving-rats.
13.Walker, J. D. et al. Chronic wireless neural population recordings with common marmosets. Cell Rep. 36, 109379 (2021).
14.Compact wireless neural recording system for small animals using silicon-based probe arrays | Semantic Scholar. https://www.semanticscholar.org/paper/Compact-wireless-neural-recording-system-for-small-Ruther-Holzhammer/1da64df729f486afb0e1fff6aa9339e7328ce7ff.
15.Interference-free, lightweight wireless neural probe system for investigating brain activity during natural competition. Biosens. Bioelectron. 195, 113665 (2022).
16.Cohen, L., Vinepinsky, E. & Segev, R. Wireless Electrophysiological Recording of Neurons by Movable Tetrodes in Freely Swimming Fish. JoVE J. Vis. Exp. e60524 (2019) doi:10.3791/60524.
17.Senkov, O., Mironov, A. & Dityatev, A. A novel versatile hybrid infusion-multielectrode recording (HIME) system for acute drug delivery and multisite acquisition of neuronal activity in freely moving mice. Front. Neurosci. 9, (2015).
18.Hong, N. et al. Machine learning-based high-frequency neuronal spike reconstruction from low-frequency and low-sampling-rate recordings. Nat. Commun. 15, 635 (2024).
19.Liang, Y., Shi, W., Hu, D., Xiang, A. & Zhang, L. Protocol for recording the discharge of locus coeruleus neurons in free-moving mice during different sleep-wake stages. STAR Protoc. 2, 100981 (2021).
20.Mishra, V., Gautier, N. M. & Glasscock, E. Simultaneous Video-EEG-ECG Monitoring to Identify Neurocardiac Dysfunction in Mouse Models of Epilepsy. J. Vis. Exp. 57300 (2018) doi:10.3791/57300.

发表回复